肝细胞癌(HCC)是全球癌症致死的主要原因之一,其治疗一直面临严峻挑战。射频消融(RFA)作为一种微创治疗手段,因创伤小、可重复性强且成本相对较低,已成为早期HCC的重要治疗方式,其局部控制效果与手术切除相当。然而,临床中常见的不完全消融(iRFA)问题,往往导致肿瘤局部复发和转移,严重影响治疗效果。研究表明,m6A RNA甲基化阅读蛋白YTHDF1在这一过程中扮演关键角色,但此前缺乏能够特异性抑制YTHDF1并阻断iRFA后肿瘤复发的有效手段。
针对这一难题,闫飞教授团队成功构建了一种基于镓金属有机框架(Ga-MOF)的“双阶段累积激活”自噬降解系统——GaMOF@M-Beclin-Y040。该系统以肝癌细胞膜进行仿生修饰,并通过代谢糖基工程与点击化学技术,将YTHDF1特异性小分子抑制剂Y040与自噬激活肽Beclin-1精准组装于材料表面。
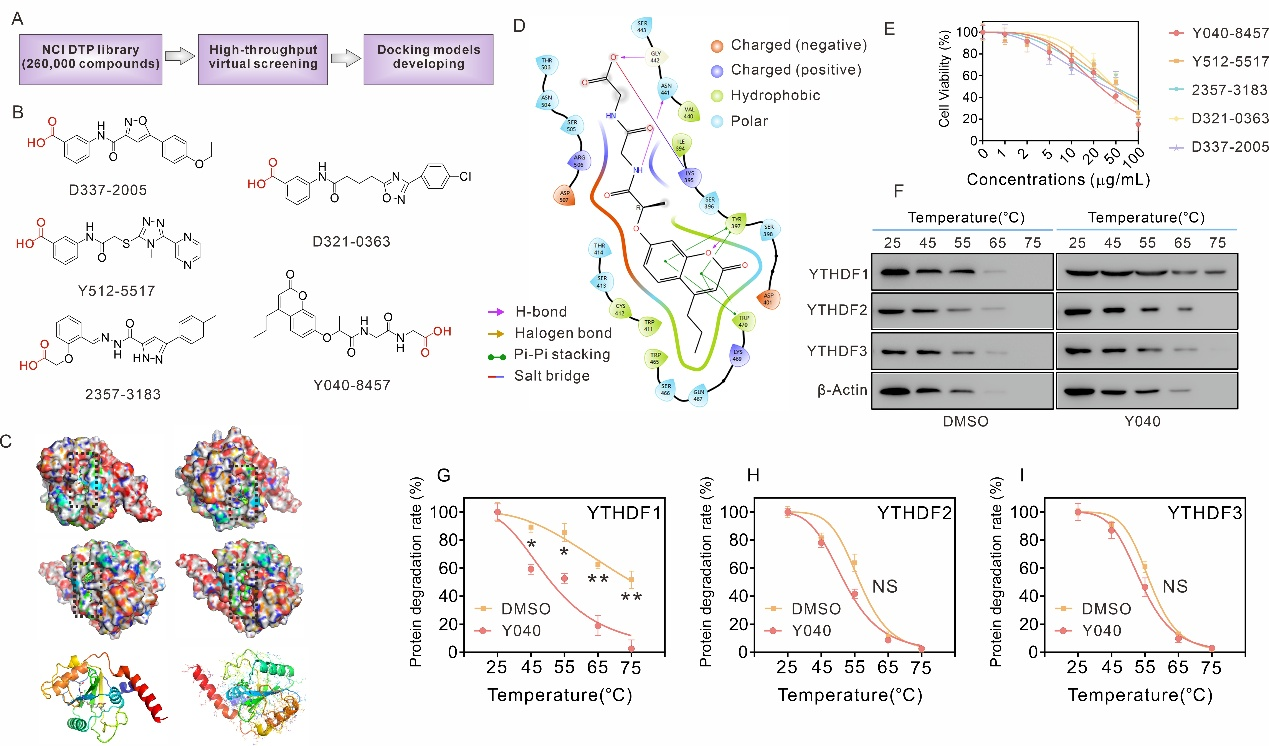
图1. YTHDF1特异性小分子结合剂Y040的筛选。
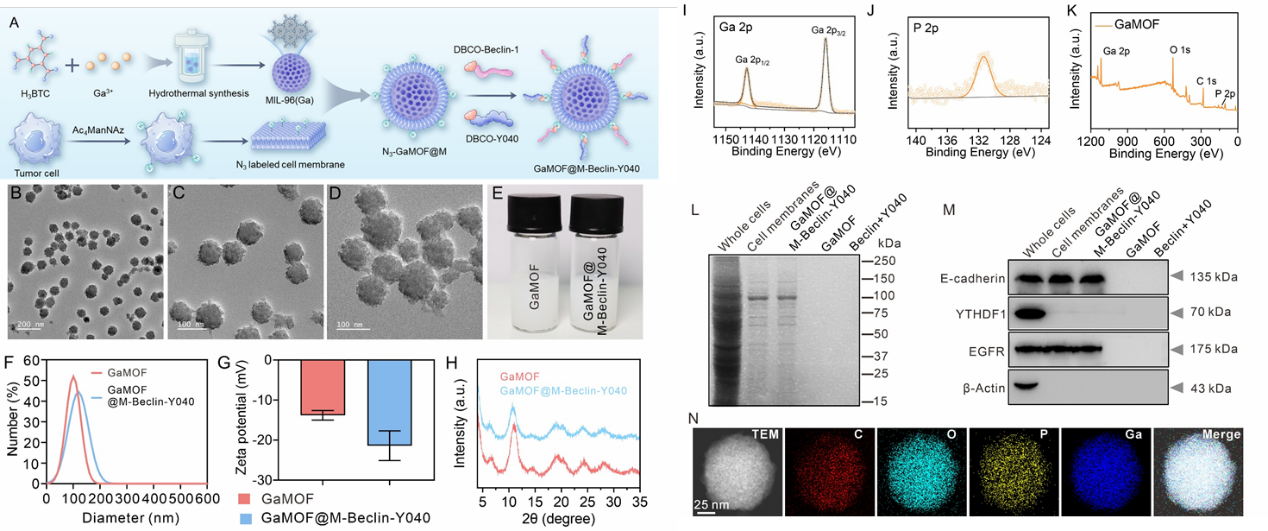
图2. GaMOF@M-Beclin-Y040的合成与表征。
研究显示,该仿生系统可将肝癌细胞的自噬通量提升7.1倍,并实现高达92%的YTHDF1选择性降解。这一过程进而显著降低了表皮生长因子受体(EGFR)的m6A依赖性转录稳定性及其蛋白表达水平,同时诱导肿瘤细胞发生免疫原性细胞死亡(ICD)。
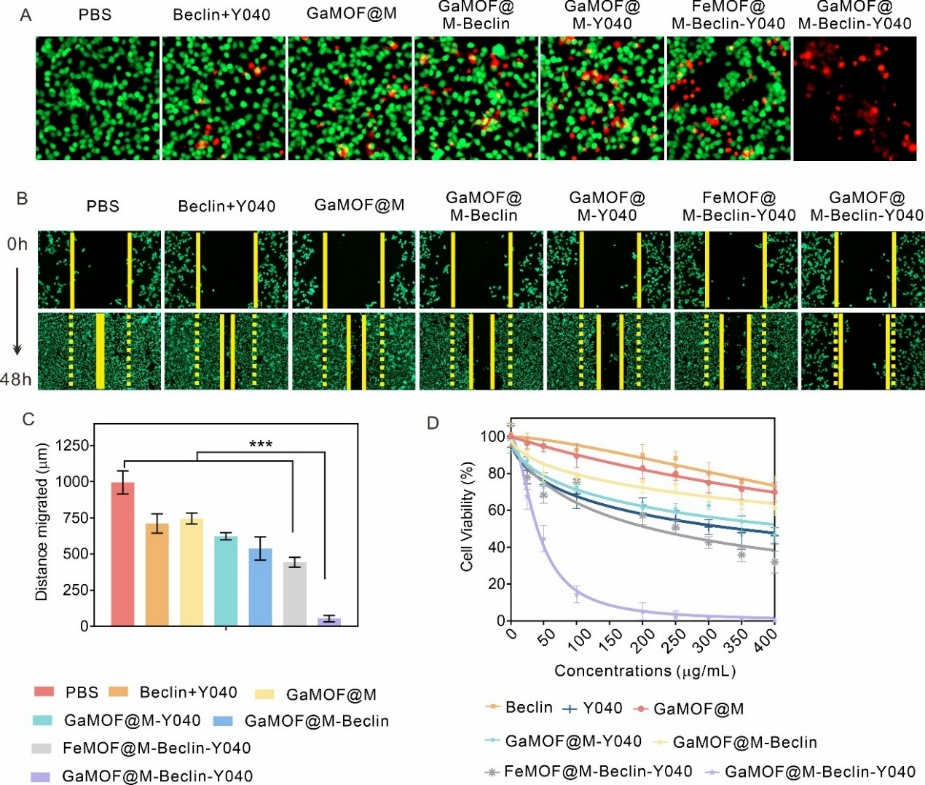
图3. GaMOF@M-Beclin-Y040的体外抗肿瘤活性
在三种不同的肝癌动物模型中,GaMOF@M-Beclin-Y040能够在iRFA后高效抑制局部肿瘤复发,抑制率达93.4%;若与抗PD-1抗体联用,更可将转移性肿瘤的生长抑制率提升至96.6%。尤为重要的是,该系统能够诱导产生持久的免疫记忆效应,使肿瘤复发率降至7.5%。
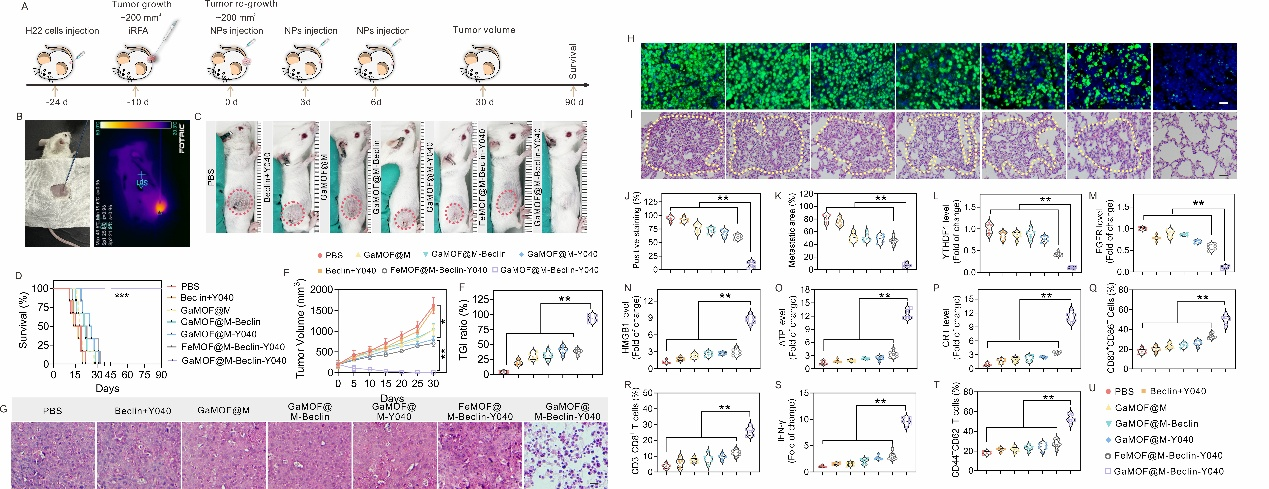
图4. GaMOF@M-Beclin-Y040有效抑制iRFA后HCC的复发。
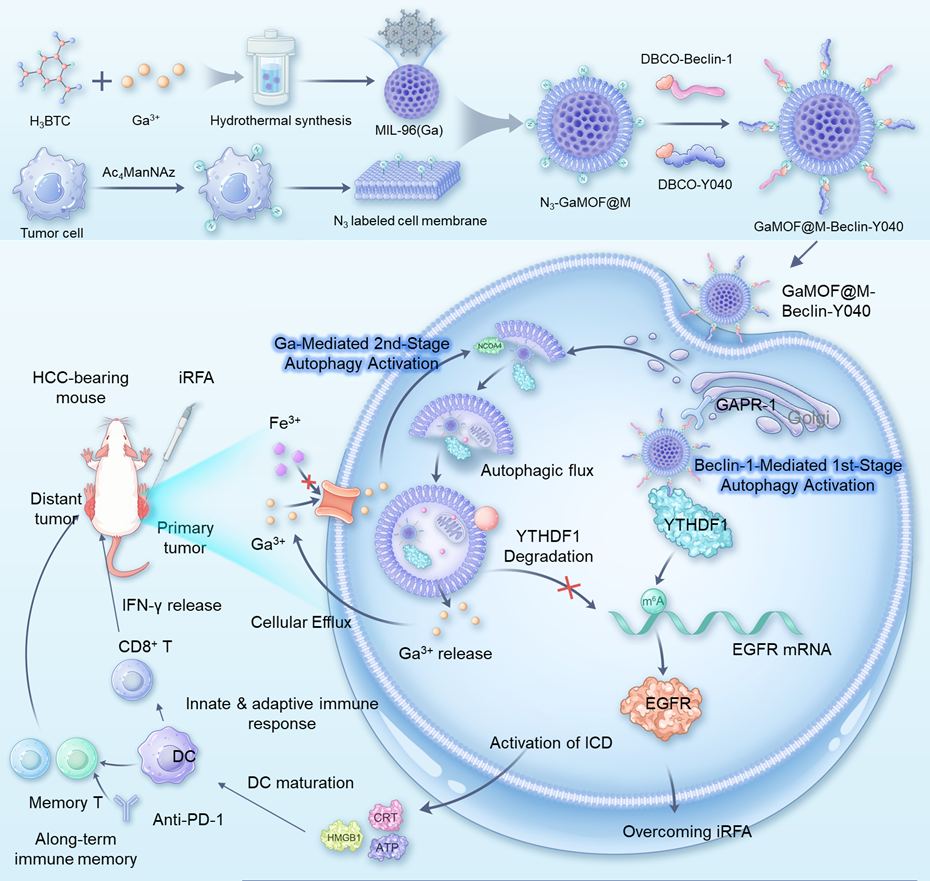
图5. 基于仿生MOF材料构建的“二阶段累积激活”自噬降解系统,用于克服HCC的不完全射频消融(iRFA)治疗难题。
该研究不仅为应对iRFA后肿瘤复发提供了创新性解决方案,也为靶向传统“难成药”靶点的肿瘤治疗开辟了新路径。相关成果以“A Biomimetic MOF-Based ‘Dual-Stage Cumulative Activation’ Autophagic Degradation System to Counter Tumor Recurrence Following Incomplete Radiofrequency Ablation of Hepatocellular Carcinoma”为题,发表在期刊Advanced Materials上。吉林大学化学学院博士毕业生王艺桥为论文第一作者,闫飞教授与白求恩第一医院戴昕伦医师为本文通讯作者。
本文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202513577